長期感染武漢肺炎,一個人體內的病毒演化生死鬥 原載於泛科學
COVID-19(武漢肺炎、新冠肺炎)全球廣傳一年下來,已經有很多億人得疫。多數人感染不久之後,便順利消滅入侵的 SARS二世冠狀病毒(SARS-CoV-2),少數人拖比較久,甚至持續數個月。 一位長期感染的英國病人,提供病毒演化的寶貴線索。

圖/Alamy
免疫力低落,長期感染的患者
追蹤病毒如何演化,兼具學術與應用價值。一位長期感染的患者,體內病毒衍生出豐富的遺傳多樣性,彼此競爭激烈,還受到抗體療法影響。此一罕見病例,讓我們見識到病毒演化與適應的可能性。
這位住在英國的先生,2012 年診斷出淋巴瘤,經歷化療,有缺乏 B細胞、T細胞等免疫缺陷的狀況,瘟疫肆虐下可謂高風險人士。2020 年夏天他感染 SARS二世冠狀病毒,由於多重器官衰竭在第 102 天去世。[1]
他一開始感染的病毒應該只有一個來源,除了相當常見,S蛋白質(spike protein)上的 D614G 突變之外(Spike(D614G)),沒有特別值得一提的特徵。
*遺傳變異的表示法為:蛋白質名稱(原本的氨基酸、突變位置、改變後的氨基酸)。如 Spike(D614G) 意思是 Spike 蛋白質上,第 614 個氨基酸,從天門冬胺酸(aspartic acid,D)變成甘胺酸(glycine,G)。
他在不同日期的 Ct值介於 16 到 34,一直到去世時體內仍有病毒。比較 23 個時間點,採檢口鼻獲得樣本的遺傳定序,讓我們有機會追蹤同一個人長期感染下,病毒演化的寶貴資訊。
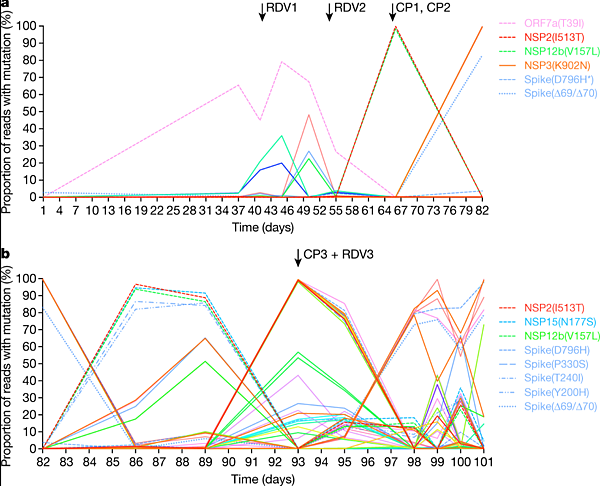
不同遺傳特徵的病毒們,在不同日期的比例變化。起伏相當劇烈。圖/[參考資料1]
今天完全執政,十幾天後一席不剩
第一個明顯的遺傳變異,是出現在 ORF7a 蛋白質上的 T39I 突變(ORF7a(T39I))。它占樣本中所有病毒的比例逐漸增加,第 37 天突破 60%,隨後降低到 40%,第 45 天又衝上 79% 的巔峰,接著逐漸減少,第 55 天跌落到 30%,第 66 天趨近於零。
患者從第 41 天、第 54 天起,兩度連續 10 天接受瑞德西韋治療,是影響病毒演化的一項因素;但是病毒的演化,不見得都和瑞德西韋有關。
第一次使用瑞德西韋之前幾天,已經有幾個突變出現,接著不同變異有升有降。最大幅度的變化是位於 NSP2 蛋白質的 I513T(NSP2(I513T))及 RdRp 蛋白質的 V157L(RdRp(V157L)),它們在第 54 天時幾乎不存在,接下來電梯向上,第 66 天時直逼 100%,徹底取代之前的 ORF7a(T39I)。
這幾天發生的一個插曲是,位於 S蛋白質上的 N501Y,也在這位患者體內誕生。它在世界各地屢屢獨立出現,包括知名的英國、南非、巴西新型病毒皆有配備。紀錄如此輝煌的它,第 55 天時存在感還有 33%,但是不敵 NSP2(I513T) 和 RdRp(V157L) 的組合,10 天後慘遭完全淘汰。
然而,NSP2(I513T) 和 RdRp(V157L) 組合也無法長期執政,第 66 天攀上 100% 的頂點後,第 82 天又跌到幾近不存。這群病毒間的競爭實在激烈!之所以如此,應該和血漿抗體療法有關。
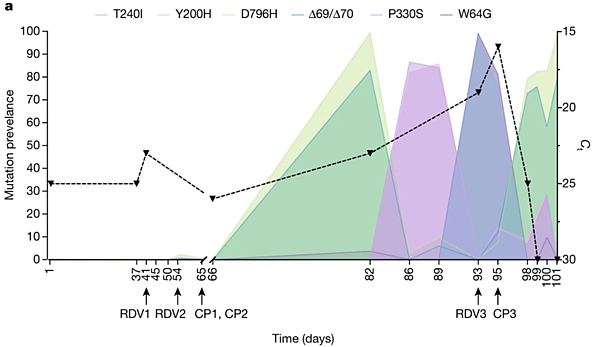
病毒 S蛋白質上的不同遺傳變異,在不同日期的比例變化。在血漿抗體療法過後,位於 S蛋白質上的各種遺傳變異,突變數量和佔整體比例都迅速增加。圖/[參考資料1]
改變局勢的外來抗體
人感染病毒後,會產生對抗病毒的抗體;這些抗體不只一種款式,針對病毒的不同目標攻擊,被稱為多株抗體。康復後一段時間,多株抗體仍然存在血漿中;將這些抗體抽血取出,給予正在感染的患者,可能有治療的作用。
這位英國先生在第 63 和 65 天,各進行過一次血漿抗體療法,結果劇烈地影響病毒生態。NSP2(I513T) 與 RdRp(V157L) 組合不敵外來抗體攻擊,存在感扶搖直下,取而代之的新貴,是 S蛋白質上兩處突變的新組合。
S蛋白質可分為 S1、S2 兩部分,新組合為 S1 的缺失 ΔH69/ΔV70(Spike(Δ69/Δ70))以及 S2 的 D796H(Spike(D796H))。血漿療法過後,這組搭擋的存在感持續攀升,第 82 天時達到 80%,隨後卻迅速下跌,第 93 天跌到未滿 1%。
患者感染超過 90 天後,愈來愈多不同型號的病毒衍生而出,起落相當劇烈而迅速。久病未癒之下,患者在第 93 天接受第三次瑞德西韋,第 95 天第三次血漿療法;在此之後,原本瀕臨淘汰的 spike(D796H, Δ69/Δ70) 再次偉大。
不論病毒生死鬥曾經多麼激烈,都在宿主於第 102 天死亡後愕然而止。表面上看是一位患者的身體,被病毒盤據一百多天;但是連日取樣告訴我們: 病毒同類間的競爭極為劇烈,可能今天完全執政,十幾天後就一席不剩。
這起實例表示,一款病毒在同一個人體內發展一百天,可以衍生出十分多樣的變化,也有機會累積很多突變。不同遺傳變異的起起伏伏,也許取決於運氣,也可能競爭力確實有別。
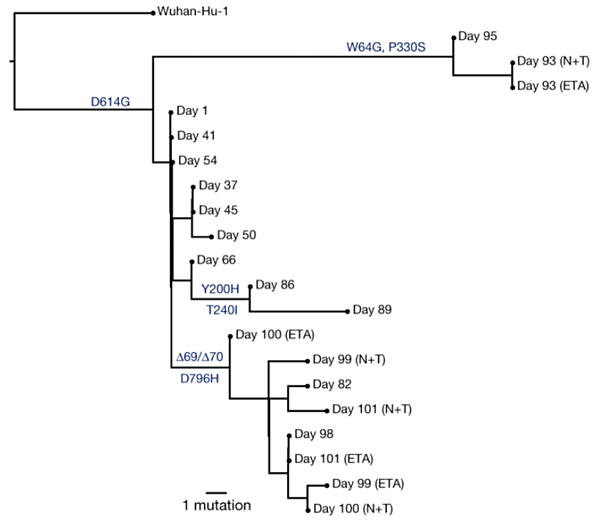
患者體內的病毒,各款衍生型號間的親戚關係。圖/[參考資料1]
專門適應抗體的突變組合
最可能有影響的,是 S蛋白質上 D796H 及 ΔH69/ΔV70 兩處變異。第 63 和 95 天兩波血漿抗體療法後,這對組合 spike(D796H, Δ69/Δ70) 的存在感皆迅速上升,令人懷疑它們更能應付抗體。
兩個突變造成什麼影響呢?體外測試發現,只有 D796H 會使感染力下降,ΔH69/ΔV70 單獨存在則能讓感染力提高 2 倍;兩者同時存在的話,感染力維持原狀。因此這款病毒的感染力可謂一增一減,整體並無增強。
以血漿中的多株抗體測試抵抗力,結果一如預期。兩者一起,或是只有 D796H 存在,都能明顯增進對付抗體的能力。僅有 ΔH69/ΔV70 時,抵抗力卻缺乏影響。
探討分子演化時必需具備的基本觀念是,遺傳改變的結果,往往不是直接的進化或退化,而是不同遺傳變異的組合,在特定情境下導致有利或有害的影響。
這兒看來就是這樣。當抗體來襲時,只有 D796H 的病毒有抵抗力,但是感染力不佳;僅有 ΔH69/ΔV70 的病毒強化感染力,卻會被抗體屠殺。兩者必需一起作用,才能在抗體造成的逆境之下,創造對同類的相對優勢,成為贏家。
然而,沒有抗體的時候,spike(D796H, Δ69/Δ70) 組合似乎毫無優勢,甚至成為被淘汰的魯蛇,原因不明。不過它面對抗體的優勢或許相當明顯,才能在跌落至未滿 1% 的苟延殘喘下,再度強勢崛起。
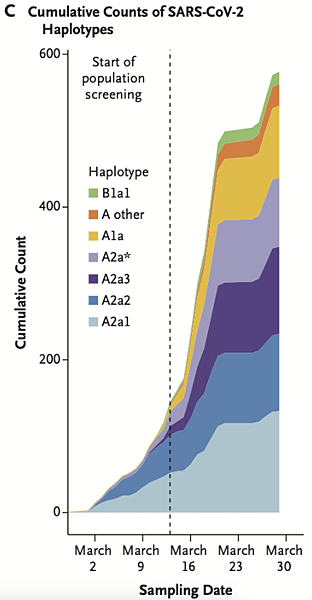
冰島在疫情初期,多款遺傳不同的病毒分別入侵,比例隨之高低起伏。英國先生只有一個人,體內病毒卻衍生出遺傳有別的許多型號,可謂一人一世界。圖/Spread of SARS-CoV-2 in the Icelandic Population
類似模式,重複出現
由於感染人數眾多,多款遺傳有別的病毒,可能同時在同一地區流傳,彼此間有競爭關係,追蹤不同時間的取樣,可以見到不同遺傳型號的波動起伏。
上述狀況,卻具體而微地發生在一位英國病人的體內;這和他原本免疫力低落,無法自製抗體,壓制病毒有關。 除了這位先生,至今還觀察到其他 4 位免疫力低落的長期感染者(平均 115 天)。這些長期感染的罕見病例,帶來認識病毒演化的珍貴線索。[2]
英國先生之外,另一位感染 74 天後去世的免疫缺失病患,感染期間病毒也陸續出現新的遺傳變異;表示同一個人體內發展出共存的多款病毒,並非個案。[3]
每一處出現突變的機率,通常沒有太大差異;是否能夠留下,發展如何,則受到天擇影響。 突變單獨出現,和組合存在的效果有時候不一樣,S蛋白質上的 D796H 與 ΔH69/ΔV70 就是如此。
另外多次重複誕生,有助於對付抗體的突變 E484K,似乎也需要 N501Y 同時存在,才能維持感染力。根據這些觀察推論: 某些突變之間有關聯性,當一個突變誕生後,另一個特定突變出現而留存的機率將會大增。

世界各地不同病毒,S蛋白質關鍵區域出現的突變們。有數個突變,在不同地區獨立出現過。B.1.1.7 首先在英國偵測到、B.1.351 在南非、P.1 在巴西、A.23.1 在烏干達、B.1.525 在奈及利亞、B.1.429 在加州、B.1.526 在紐約。圖/[參考資料2]
實際見到讓病毒加速改變的「總加速師」?
瘟疫蔓延一年後,觀察得到一項發現:許多獨自演化的病毒們,S蛋白質產生類似的變化。類似改變重複出現,揭示病毒適應的可能性,與侷限性。
存在感在 2020 年底迅速增加,而引起注意的三款新型病毒:英國首度發現的 B.1.1.7、南非的 B.1.351、巴西的 P.1,出現時間都在前述 5 位長期感染的患者之後,和他們沒有關係。
三款新型病毒的 S蛋白質也出現多處突變,基因組其餘位置累積的突變數則更多,如 B.1.1.7 和近親相比,便有 17 處新突變。過去一年多來,SARS二世冠狀病毒平均一個月約累積 2 個突變,突然冒出那麼多突變,很不尋常。
三款新型病毒的來歷不明,有人推測,它們是在免疫力低落者的體內,長期感染後,累積許多突變而成。
英國先生體內衍生的眾多型號中,第 93 天時突變數目最多的病毒,累積數量和 B.1.1.7 類似,S蛋白質上也配備 2 處突變(W64G、P330S)。此一觀察,支持新型病毒源自於總加速師的論點。
對這位拓展知識疆域,卻失去生命的英國先生,我們懷念他 QQ
堅強防線中最弱的一環,容易成為對手的突破點,必需特別保護。圖/Wikimedia Commons
保護群體最弱的人,才能保護整體
認識病毒的演化過程,以及潛在的適應方向,有助於藥物、抗體和疫苗的研發。治療和疫苗,人為創造出病毒的逆境,也無可避免地會篩選出抵抗力更強的品系;所幸有些策略,能夠反制抵抗力。
相對地,不必要的拖延或不當措施,例如錯誤使用不佳的疫苗,也會增加病毒適應的機率,必需避免。
長期感染,令病毒有更多機會累積突變,適應各種逆境。因此必需減少長期感染的人數,尤其要盡量避免免疫力低落者感染,想辦法保護他們;萬一感染,也要特別謹慎治療,以免有變強的新型號病毒竄出。
防線即使堅強,最弱的環節卻容易先被突破。保護群體中最弱的人,才能保護整個群體。
WARS無症狀感染者,會傳染,隔離14天可以拖到傳染高峰過去
在世界各地都取得優勢,不只是運氣好?——冠狀病毒的D614G突變(上)
結構強化的病毒,傳染力更強——冠狀病毒的D614G突變(下)
病毒不是源於武漢的海鮮市場?從分子演化學角度看2019新型冠狀病毒(武漢肺炎)的起源與傳播
1. Kemp, S. A., Collier, D. A., Datir, R. P., Ferreira, I. A., Gayed, S., Jahun, A., … & Gupta, R. K. (2021). SARS-CoV-2 evolution during treatment of chronic infection. Nature, 1-10.
2. The emerging plasticity of SARS-CoV-2
3. Hensley, M. K., Bain, W. G., Jacobs, J., Nambulli, S., Parikh, U., Cillo, A., … & Haidar, G. (2021). Intractable Coronavirus Disease 2019 (COVID-19) and Prolonged Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Replication in a Chimeric Antigen Receptor-Modified T-Cell Therapy Recipient: A Case Study. Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America.
歡迎光臨粉絲團一起討論:盲眼的尼安德塔石器匠


 留言列表
留言列表
 科學資源
科學資源 
